Princípios de espectroscopia de infravermelho (1)
Princípios de espectroscopia de fluorescência (5)
6 de outubro de 2020Princípios de espectroscopia de infravermelho (2)
6 de outubro de 2020Princípios de espectroscopia de infravermelho (1)
Vibrações moleculares e absorção infravermelho
O que é absorção infravermelho?
Em espectroscopia infravermelho, uma amostra é irradiada com luz infravermelho, e a luz refletida ou transmitida é medida, com isso é possível que se realizem análises estruturais e quantificações. Análises relativas à absorbância se referem à capacidade de uma molécula de absorver a luz irradiada e, portanto, são dependentes de um comprimento de onda. Neste caso, a exposição a luz resulta em transições eletrônicas. Em contraste, a luz infravermelho (2.5 a 25 µm) é absorvida, promovendo vibrações e rotações em moléculas, transições estas que necessitam de menor energia, como pode ser observado na figura 1.
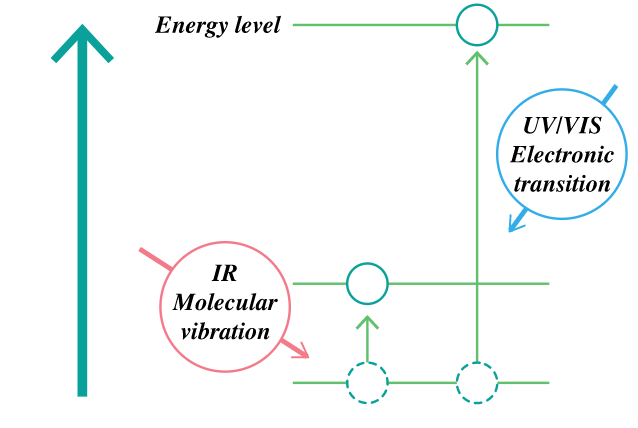
Fig. 1 Comparison of infrared and UV/VIS absorption
Comparativo de absorção infravermelho e UV/Vis
Vibrações moleculares e absorção infravermelho
As ligações químicas entre átomos que compõe uma molécula podem se esticar como molas. A energia relacionada a este tipo de vibração de deformação axial é muito próxima à da radiação infravermelho, o que permite a sua absorção e subsequente movimentação. As vibrações apreciáveis por infravermelho são limitadas àquelas que envolvem mudança de dipolo. A absorção infravermelho não ocorre em situações em que vibrações moleculares se anularão.
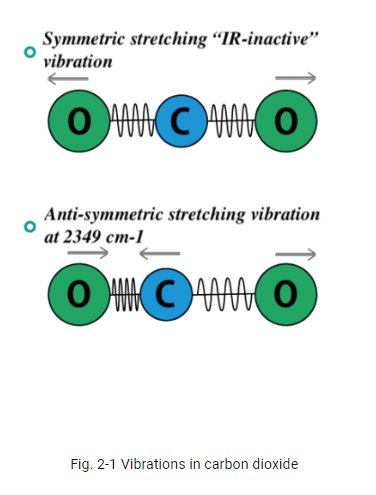
Analisando uma molécula como o CO2, é impossível que se observe a absorção de radiação infravermelho considerando uma vibração de deformação simétrica, uma vez que não há mudança de dipolo. Por outro lado, deformações axiais assimétricas são perceptíveis, uma vez que geram mudanças desta natureza, como representado na figura 2. O Aquecimento da atmosfera acontece devido à absorção de radiação infravermelho desta maneira apresentada, classificando-o como um gás de efeito estufa.
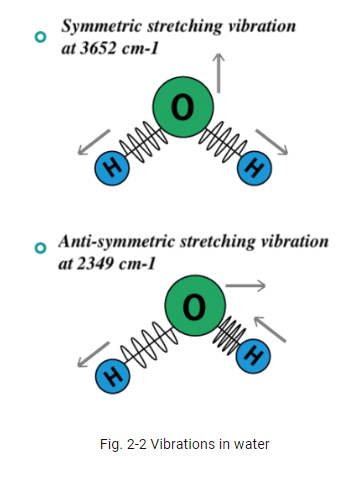
No caso da água, uma molécula não linear, pode-se observar absorção infravermelho tanto nas deformações simétricas e assimétricas, devido à alteração de dipolo. A banda de absorção referente à deformação simétrica pode ser encontrada em 3,652 cm-1 e a assimétrica em 3,756 cm-1, como observa-se na figura 2.
Identificação de moléculas
Em um espectro infravermelho, sinais de absorção são associados à grupos funcionais como -OH e -COOH, observados em faixas de número de ondas específicas. Tais regiões são reconhecidas como bandas de absorção características, analisadas e utilizadas para estimativas de estrutura química de uma molécula. O espectro infravermelho apresenta informações únicas de um composto e pode ser comparado com bases de dados contendo amostras de padrões de diversas moléculas de maneira a identificar uma substância desconhecida. Atualmente existem milhares de espectros disponíveis em bases de dados. Estas bibliotecas possuem espectros em sua maioria de moléculas orgânicas e podem ser utilizados para diversos fins, como na medicina, agricultura, biologia, análises forenses, de gases, síntese orgânica, ente outros.

