
Fluorescência é um tipo de fotoluminescência, efeito que se refere a todo tipo de processo de reemissão de luz depois da absorção de fótons. Diferente de reflexão ou espalhamento, o comprimento de onda da luz emitida é maior do que o absorvido pelo material. Quando um material fluorescente ou fosforescente é irradiado com luz ultravioleta de alta energia, este entra em um estado de excitação devido a transições eletrônicas. A luminescência ocorre quando elétrons retornam de um estado excitado para seu estado fundamental. Um exemplo de organismo que emite luminescência é Aequorea Victoria apresentada na figura 1. Luminescência é um termo genérico para emissão de luz seguido de absorção de energia ótica (tabela 1).
| tipo | fonte | exemplo |
| Fotoluminescência | Radiação UV, visível e infravermelho | Fluorescência e fosforescência |
| Luminescência química | Reação química, oxidação | Fósforo branco, formaldeído, paraldeido em solução etanol/álcali, oxidação de siloxeno por Ce (IV) |
| Eletroluminescência | Campo elétrico | LED, eletroluminescência orgânica ou inorgânica |
| bioluminescência | Adsorção fisiológica, oxidação enzimática | Luminescência observada em vagalumes devido à oxidação catalítica da luciferase |
| radioluminescência | Raios α/β/γ, nêutrons | Cintilador (NaI · TII) |
| Luminescência de raio-X | Raio-X | Interações com ZnCdS: Ag, ZnS: Ag |
| catodoluminescência | Feixe de elétrons | fósforo, tubo de raio catódico para CRT, apatita |
| termoluminescência | aquecimento | Luminescência devido à altas temperaturas (fluorita, sulfeto de fósforo) |
| sonoluminescência | Ondas sonoras ou ultrassom | Reações químicas pelo estímulo sonoro (reação de oxidação do luminol) |
| triboluminescência | Fricção ou destruição | Cristais de açúcar, ZnS |
Tabela 1 tipos de luminescência
A energia contida em um fóton pode ser expressa por E = hν (onde E é energia, h é a constante de Planck e v é a frequência). Quando a luz atinge uma substância, esta é absorvida por elétrons de modo a gerar mudanças de composição eletrônica de um estado fundamental estável para um estado excitado de maior energia. A luminescência ocorre quando a energia é liberada na forma de emissão de luz ao invés de vibrações ou geração de calor. A configuração eletrônica retorna ao estado fundamental como demonstra a figura 2. Em muitos casos, parte da energia absorvida é emitida como energia térmica, de forma que a luz emitida apresente um comprimento de onda maior do que da luz emitida (deslocamento de Stokes).
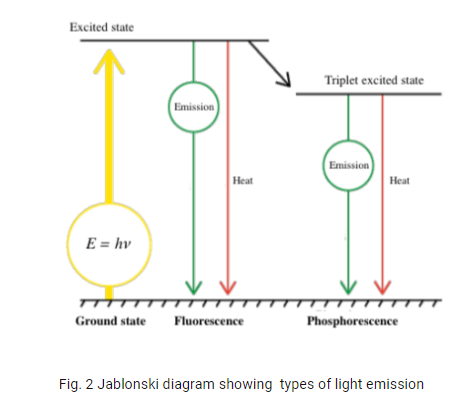
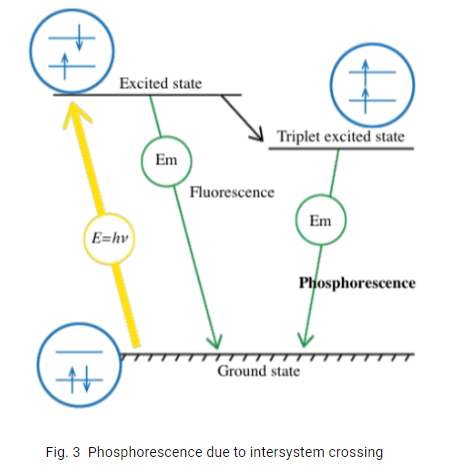
Emissão de luz como resultado de foto-excitação pode ocorrer parcialmente na forma de fluorescência e parcialmente na forma de fosforescência. A fosforescência ocorre como resultado de um cruzamento entre sistemas, de modo que os elétrons sejam impossibilitados de retornar ao estado fundamental diretamente, realizando uma transição para um estado intermediário. O lento relaxamento que culmina no retorno ao estado fundamental é reconhecido como fosforescência.
A fluorescência ocorre em uma escala de nanosegundos, ao contrário da fosforescência que pode continuar por períodos maiores. Quando transições eletrônicas ocorrem em uma substância, pares de elétrons geralmente possuem “spins” opostos (princípio de exclusão de Pauli). No entanto, quando um cruzamento intersistêmico ocorre, os spins são iguais. Uma vez que este é um “estado proibido”, o relaxamento para o estado fundamental é lento.

Receba o conteúdo da Jasco Brasil direto no seu e-mail.